结直肠癌(colorectal cancer,CRC)包括发生在结肠或直肠的恶性肿瘤,是癌症死亡的主要原因之一,占全球死亡人数的9.2%[1]。作为一种多模式疾病,CRC与相关信号通路的异常激活、免疫破坏等有关[2]。目前CRC的治疗策略主要以放化疗、免疫治疗和手术治疗为主,面临着从癌症复发和耐药性到明显毒性的挑战。因此,迫切需要对CRC患者进行更有效的治疗。
黄酮类化合物是天然有机化合物的重要组成成分,已被报道的黄酮类化合物的结构超过10000种[3]。此外,黄酮类化合物以副作用小、逆转化疗耐药性的特点展现出巨大优势,已被视为CRC潜在的治疗药物[4]。然而,目前尚缺乏黄酮类化合物治疗CRC的相关综述。现对黄酮类化合物治疗CRC的文献进行归纳总结,就 PI3K/AKT、Wnt/β-catenin MAPK等主要信号通路探讨黄酮类化合物治疗CRC的作用机制,为其在CRC防治中的应用提供理论支持。
1 黄酮类化合物的结构分类
黄酮类化合物是存在于天然植物的酚类化合物,由两个酚羟基构成的苯环,常被称为苯环A和苯环B,通过3个碳原子连接在一起,构成了C6−C3−C6基本骨架结构[5](图1)。黄酮类化合物普遍存在中草药的根、茎、叶中,如葛根、黄芩等,在人类的生命活动中扮演重要的角色[6]。黄酮类化合物按苯环的不同组成,可以分为多个不同种类,包括黄酮类、黄酮醇类、异黄酮类、查耳酮类等(图2),其中黄酮和黄酮醇是最常见的形式[7]。
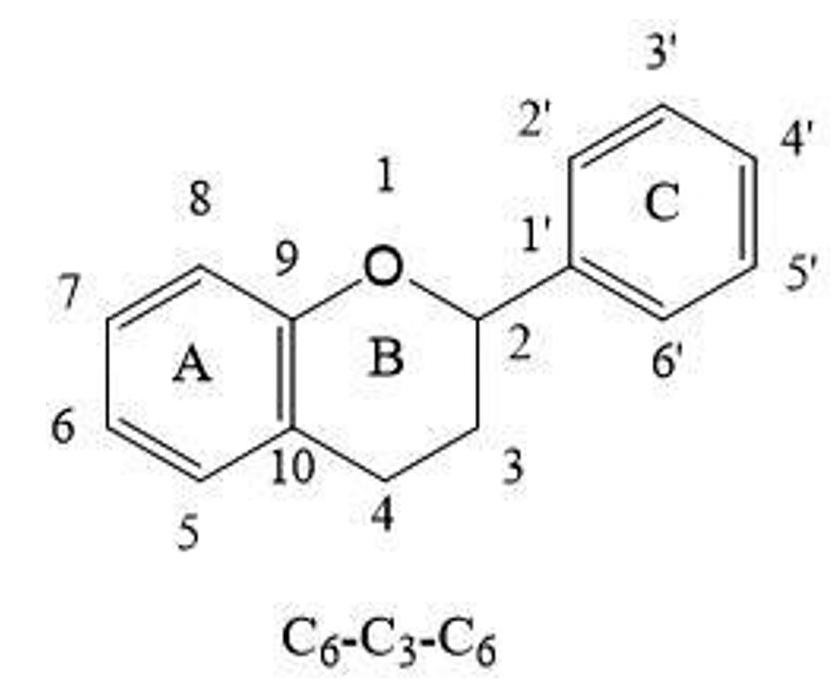
图1黄酮类化合物的基本骨架结构
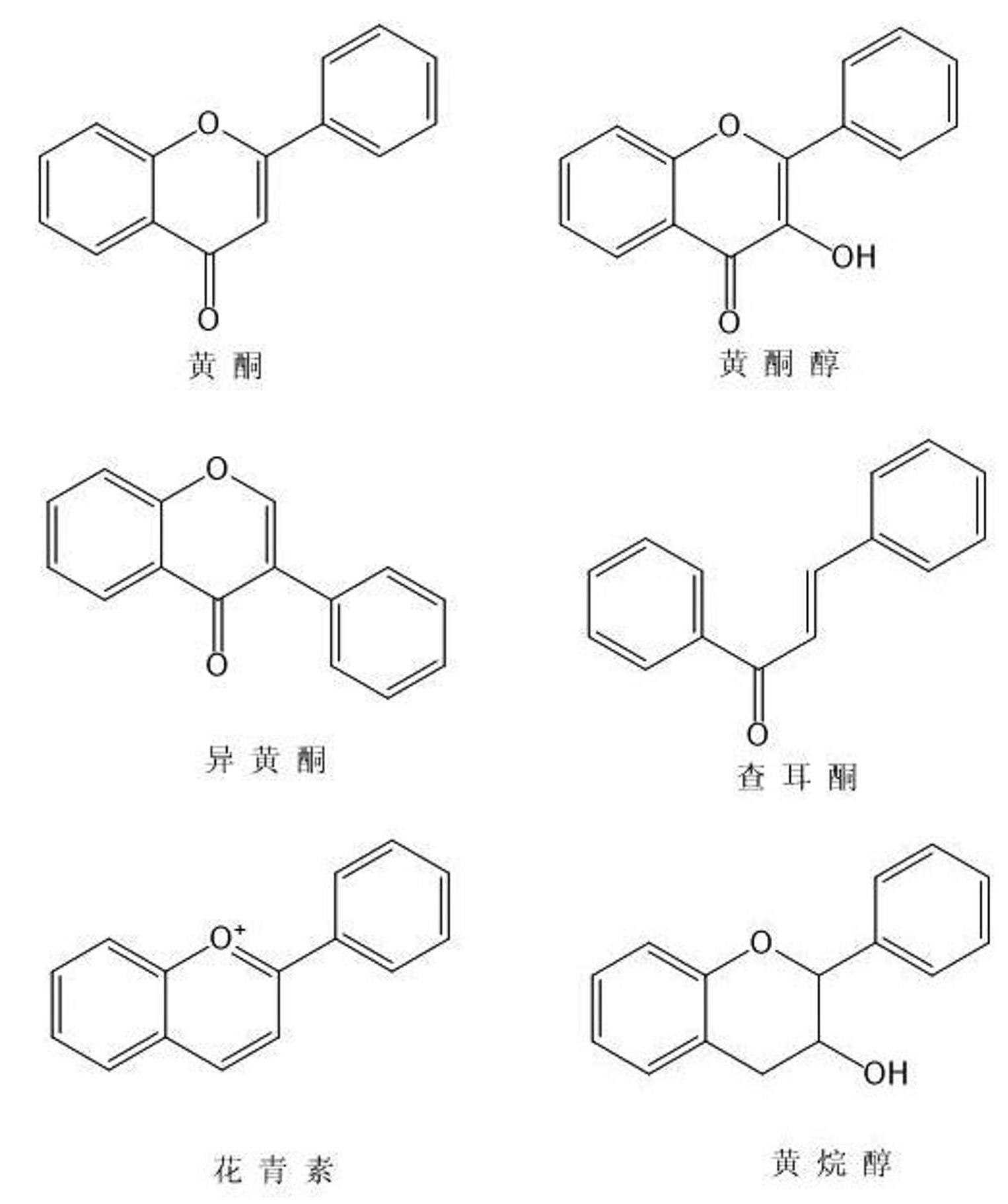
图2黄酮类化合物的结构式
2 黄酮类化合物通过PI3K/AKT信号通路抗CRC
PI3K/AKT是细胞内重要的信号通路,主要参与调节细胞的增殖、分化等生理活动[8]。PI3K 催化二磷酸脂酰肌醇(PIP2)磷酸化为三磷酸脂酰肌醇(PIP3),进而激活AKT使下游转录因子磷酸化以调控凋亡基因的表达,辅助肿瘤细胞的存活[9]。
木犀草素来源于木犀草,能够抑制基质金属蛋白酶(MMP)-2/9的活性,阻止细胞外基质的降解和重塑[10]。魏付桥等[11]研究发现,木犀草素抑制 PI3K、AKT的磷酸化负向调控MMP-9,抑制CRC 细胞的增殖、侵袭及转移。柚皮素存在芸香科植物中。Abaza等[12]研究表明,柚皮素抑制PI3K、p-AKT 的活化,改变半胱氨酸蛋白酶(Caspase)-3,7,8,9、Bcl-2相关X蛋白(Bax)和B-淋巴细胞瘤因子-2(Bcl-2)的表达,促细胞凋亡并阻滞细胞周期于 G2/M期。毛蕊异黄酮提取自黄芪的根部。李通[13]研究表明,毛蕊异黄酮抑制p-AKT的表达后导致Bcl-2下调,诱发细胞凋亡。芹菜素是黄酮类化合物,因其抗癌作用和低毒性备受青睐。实验发现,芹菜素下调PI3K、AKT的磷酸化和 p62 的表达,上调 Beclin-1、LC 3-ⅡI 的表达,从而引起Bax和 Bcl-2 的改变,诱导细胞自噬和凋亡[14]。川陈皮素可抑制 Bcl-2 表达和 AKT、mTOR 的磷酸化,促进 Bax 和 Caspase-3 的表达,增加CRC对奥沙利铂的敏感性[15]。异鼠李素是沙棘中主要的黄酮类化合物,研究表明,异鼠李素抑制 AKT的表达影响下游蛋白p70S6K 和4E一BP1的磷酸化,抑制CRC细胞的增殖并阻滞细胞周期于G2/M期[16]。
3 黄酮类化合物通过Wnt/ β-catenin信号通路抗CRC
Wnt/β-catenin信号通路分经典和非经典两类,β-catenin蛋白是经典通路中的重要组成部分[17]。重要蛋白APC基因编码腺瘤性息肉病相关蛋白(APC)失调或缺失时,可激活β-catenin蛋白易位到细胞核与T细胞因子(TCF)和淋巴增强因子(LEF)转录因子家族结合,启动下游基因的转录,促进CRC的发展[18]。
山奈酚是黄酮类化合物,可下调Axinl β-catenin、Wnt5a、Dvl2、Dvl3的表达,影响细胞周期紊乱和细胞凋亡等生物学功能[19]。花青素是植物的天然色素。Zhang 等[20]研究发现,花青素靶向miR−24−1−5p 下调β-catenin、c-Myc、cyclin的表达,最终抑制CRC 细胞增殖。水飞蓟素提取自菊科植物水飞蓟。Eo等[21]研究表明,水飞蓟素抑制β-catenin的表达和TCF4的转录发挥抗结直肠肿瘤活性。研究表明,大豆素的抑癌机制是通过改变Wnt/β-catenin信号通路中β-catenin蛋白的表达来实现的[22]。根皮素属于二氢查尔酮类化合物。古双亮等[23]研究发现,根皮素下调c-Myc、Cyclin D1、β-catenin、 p-GSK-3β/GSK-3β 的表达,上调Caspase−3、Bax 的表达,抑制 CRC 细胞增殖及促细胞凋亡。
4 黄酮类化合物通过MAPK信号通路抗CRC
MAPK信号通路与肿瘤的生长、侵袭等过程密切相关[24]。MAPK 信号通路是一个级联磷酸化的过程,其主要的信号级联Ras/Raf/MEK/ERK的异常激活,导致CRC细胞摆脱正常的生长和分化控制,进而侵袭周围组织和器官[25]
异甘草素存在于植物甘草中。王志国等[26]研究发现,异甘草素下调 JNK、ERK1/2、p38 的磷酸化和上调Caspase-3的表达以促进细胞凋亡,抑制细胞增殖、侵袭和转移。白杨素来源于紫葳科植物木蝴蝶,研究表明,白杨素上调Bax 和Caspase-3 的表达,下调p−p38、Bcl−2的表达而促细胞凋亡,抑制细胞的增殖、侵袭和迁移[27]。黄芩素是黄芩中主要的黄酮类化合物。Su等[28]研究表明,黄芩素上调DEPP、Gadd45a、Caspase-3、Caspase-9 的表达,抑制 MAPK 磷酸化,诱导细胞凋亡。鱼藤素是提取自鱼藤的异黄酮类化合物。Chen等[29]研究发现,鱼藤素通过抑制p−p38、Bcl−2的表达,上调Caspase-3、Bax 的表达来诱导细胞凋亡。
5 黄酮类化合物通过 NF−κB 信号通路抗CRC
NF−κB 是高度保守的转录因子家族,包括 NF-κB1(p50/p105)、NF-κB2(p52/p100)、RelA(p65)等基因[30]。IKK激酶复合物被激活后引起IκB 磷酸化和泛素性降解,进而释放NF−κB 发挥作用[31]。50%CRC患者存在NF−κB 信号通路的异常激活,因而调控该信号通路在临床治疗中是至关重要的[32]。
二氢杨梅素是二氢黄酮醇类化合物,研究发现,二氢杨梅素抑制NF−κB 和 Nrf2 的表达来抑制HCT116细胞增殖和结直肠癌裸鼠的肿瘤生长[33]。研究表明,染料木素降低NF-κB p65、p-NF-κB p65、Bcl-2、N-钙黏蛋白(N-cadherin)的表达,提高Caspase −3、Caspase-8、Bax、促E-钙黏蛋白(E-cadherin)的表达,逆转大肠癌上皮细胞-间充质转化(EMT),抑制CRC的侵袭、转移并诱导细胞凋亡[34]。淫羊藿苷来自小檗科淫羊藿植物。Zhang 等[35] 研究发现,淫羊藿苷抑制NF−κB、Bcl−2、Bcl−xL、cyclin D1、血管内皮生长因子(VEGF)的表达使细胞周期阻滞于G2/M期。桑辛素来源于桑属植物。研究表明,桑辛素抑制NF−κB 的表达和IKK−α、IKK-β、IκBα 的去磷酸化促细胞凋亡,阻遏 CRC 的发生发展[36]。
6 黄酮类化合物通过JAK/STAT信号通路抗CRC
JAK发生络氨酸磷酸化后招募STAT蛋白,络氨酸磷酸化的 STAT蛋白二聚化后被转运到细胞核中调节特定的基因[37]。鉴于JAK/STAT信号通路在肿瘤中的重要作用,JAK/STAT信号通路已成为药物开发的主要靶点[38]。
飞燕草素是存在于花青素的类黄酮类化合物。 Zhang 等[39]研究发现,飞燕草素抑制 JAK2、STAT3 的磷酸化和 Bcl-2、Bcl-xL 的表达, 增强 Bax、 Caspase3 的表达,从而诱导细胞凋亡。汉黄芩素是从植物黄芩中提取的重要组分。Tan 等[40]研究表明, 汉黄芩素下调 STAT3 和 Bcl-2 的表达,增加 LC3II、 Beclin-1、Bax、Caspase 3、8、9 的表达,诱导细胞发生自噬和凋亡。芒柄花黄素是存在于黄芪的异黄酮类化合物。Wang 等[41]研究发现,芒柄花黄素通过抑制 p-STAT3 的表达,减少 p-STAT3 易位到细胞核以抑制 CRC 的生长和侵袭。
7 黄酮类化合物通过Notch信号通路抗CRC
橙皮苷属于二氢酮类化合物。Singh等[44]研究发现,橙皮苷通过抑制 Notch-1、Hes-1、Hey-1 的信使核糖核酸(mRNA)和蛋白的表达,对CRC 细胞产生毒性。芦丁又名芸香苷,研究显示,芦丁通过抑制大肠癌干细胞 CR-CSCs 中 Notch-1、Hey-1、Hes-1的表达抑制 CR-CSCs增殖,诱导 CR-CSCs 凋亡和分化[45]。槲皮素是黄酮类化合物。Li等[46]研究发现,槲皮素联合放疗显著下调Notch-1、Jagged-1、Hes-1、Hey-1的表达,抑制细胞增殖和诱导细胞凋亡。
8 黄酮类化合物通过 Hedgehog 信号通路抗 CRC
灯盏花乙素是来源于植物灯盏花的黄酮类化合物,研究表明,灯盏花乙素通过下调 Hedgehog 信号通路活性抑制结直肠肿瘤干细胞(HT-29CSC)在体内内外的分化[49]。表没食子儿茶素没食子酸酯是来源于茶叶的黄酮醇类化合物。Ding等[50]研究发现,表没食子儿茶素没食子酸酯通过抑制 SMO、Gli-1、Bcl-2的表达,上调Bax的表达来抑制细胞增殖和诱导细胞凋亡,同时抑制结肠癌裸鼠的肿瘤生长。
9 黄酮类化合物通过多条信号通路抗CRC
不同的信号通路之间非独立存在,而是相互关联,共同组成复杂的调控网络。黄酮类化合物可通过调控多个信号通路实现多靶点、多通路协同治疗CRC的效果。
红景天苷是红景天的提取物。Hao 等[51]研究发现,红景天苷可下调 p-PI3K、p-AKT、N-cadherin 的表达,上调E-cadherin 的表达,从而抑制EMT和细胞增殖、迁移、侵袭。此外,El-Kott 等[52]实验表明,红景天苷还降低 STAT3和NF−κB p65的表达,提高Caspases3、8的表达,抑制细胞增殖和诱导细胞凋亡。豆蔻明是黄酮类化合物,不仅能够下调NF−κB 的表达以抑制结肠炎相关结肠癌(CACC)细胞增殖,还能下调 p-JAK2、p-STAT1、p-STAT3 和p-STAT5的表达诱导CACC细胞凋亡[53-54]。桑黄素来源于桑橙等植物的叶子,能够下调p65-NF-κB、p-p65-NF-κB、β-catenin 的表达抑制下游靶点c-Myc、cyclin D1,从而靶向肿瘤代谢发挥抗肿瘤活性[55-56]。
10 总结与展望
上述证据提示各种相关信号通路的激活是导致CRC发生的机制之一。目前发现黄酮类化合物可通过不同靶点调控相关信号通路,进而影响细胞周期,抑制CRC增殖、侵袭、迁移,诱导细胞自噬和凋亡,逆转EMT,还能提高放化疗的敏感度,从而遏制CRC 的进程。黄酮类化合物调控相关信号通路对CRC的作用机制总结见表1,黄酮类化合物调控多条相关信号通路对CRC的作用机制总结见表2,涉及的信号通路包括PI3K/AKT、Wnt/β-catenin、MAPK等。
由于黄酮类化合物的多样性和复杂性,目前对黄酮类化合物调控相关信号通路治疗CRC的研究难以全面分析,深入性和系统性还有待加强。此外,黄酮类化合物治疗CRC的研究目前多以单味中药为主,缺少对中药复方的研究,具有较大的局限性。综上,黄酮类化合物对调控相关信号通路治疗CRC仍存在一定的局限和难点,但相信随着医药技术的发展,黄酮类化合物治疗CRC的作用机制的研究将日益深人,有待为CRC的临床治疗提供新思路。
表1黄酮类化合物靶向相关信号通路治疗CRC的作用机制

注:↑表示促进或上调;↓表示抑制或下调
表2黄酮类化合物靶向多条相关信号通路治疗CRC的作用机制

注:↑表示促进或上调;↓表示抑制或下调



