摘要
目的:研究黄芪多糖(APS)在肝癌铁死亡机制的调控作用。方法:取不同浓度APS(0、50、100、200 mg/L)处理肝癌HepG2细胞48 h,分别记作对照组和APS低、中、高剂量组。采用CCK-8试剂盒检测细胞增殖情况,同时采用试剂盒检测各组细胞的谷胱甘肽(GSH)、活性氧自由基(ROS)和脂质过氧化物水平,采用流式细胞术检测各组细胞的铁离子水平。通过蛋白质印迹法检测各组细胞的铁死亡标志蛋白谷胱甘肽过氧化物酶4(GPX4)、长链脂酰CoA合成酶4(ACSL)以及Wnt/β-catenin信号通路关键蛋白Wnt和β-catenin蛋白的表达水平。结果:与对照组相比,APS高、中、低剂量组均能抑制肝癌HepG2细胞的增殖,且随着APS的浓度升高,抑制效果更显著(P<0.05)。与对照组相比,高、中、低剂量组均能降低肝癌HepG2细胞中GSH水平,并提高ROS和脂质过氧化物水平,同时提高铁离子水平,且随着APS浓度升高效果更显著(P<0.05)。同时,与对照组相比,APS高、中、低剂量组均能降低GPX4蛋白表达水平,提高ACSL4蛋白表达水平,且呈剂量依赖性(P<0.05)。与对照组相比,APS高、中、低剂量组均能降低Wnt和β-catenin蛋白表达水平,随着APS剂量升高,蛋白表达抑制效果更显著(P<0.05)。结论:APS通过增强ROS和脂质过氧化物的积累增强铁死亡,抑制肝癌细胞的增殖,这一过程可能与Wnt/β-catenin信号通路的抑制相关。
关键词
Abstract
Objective To investigate the regulatory effect of astragalus polysaccharide (APS) on ferroptosis mechanism of hepatocellular carcinoma. Methods HepG2 cells were treated with different concentrations of APS (0, 50, 100, 200 mg/L) for 48 hours, and were recorded as control group and APS low, medium and high dose group, respectively. Cell proliferation was detected with CCK-8 kit, while glutathione (GSH), Reactive Oxygen Species (ROS) and lipid peroxide levels of each group were detected with commercial kits, respectively. Flow cytometry was used to detect theiron level in each group. Glutathione Peroxidase 4 (GPX4) and long-chain acyl-CoA synthetase 4 (ACSL4), markers of ferroptosis, were detected by Western blot, as well as the expression levels of key proteins of the Wnt/β-catenin signaling pathway including Wnt and β-catenin. Results Compared with the control group, APS high-dose, medium-dose and low-dose groups could inhibit the proliferation of HepG2 cells, and the inhibitory effect was more significant with the increase of APS concentration (P<0.05). In addition, compared with the control group, the high, medium and low dose groups could reduce the GSH level in HepG2 cells, increase the ROS and lipid peroxide levels, and increase the iron level, and the effect was more significant with the increase of APS concentration (P<0.05). At the same time, Western blot further verified that compared with the control group, APS high, medium and low dose groups could reduce GPX4 protein expression level and increase ACSL4 protein expression level in a dose-dependent manner (P<0.05). Compared with the control group, the expression levels of Wnt and β-catenin protein in high, medium and low dose APS groups were decreased, and the inhibitory effect of protein expression was more significant with the increase of APS dose (P<0.05). Conclusion APS can enhance the accumulation of ROS and lipid peroxides, enhance ferroptosis and inhibit the proliferation of hepatocellular carcinoma cells, which may be related to the deactivation of Wnt/β-catenin signaling pathway.
肝癌被称为全球第六大癌症,其致死率位居全球第三。根据2020年全球癌症统计数据可知:在中国,有超过4.1万例新发肝癌患者和3.9万例死亡患者[1]。由此可见,肝癌的发生对人类的健康和生存的威胁日益严重。因此,研究肝癌的发生机制对于肝癌的防治具有重要意义。铁死亡是一种铁离子依赖性的细胞程序性死亡方式,其特征是细胞内脂质过氧化物积累和氧化还原平衡紊乱。越来越多的研究发现促进铁死亡可抑制肝癌发展,因此,铁死亡有望成为肝癌发生机制的研究靶点[2]。黄芪多糖(astragalus polysaccharide,APS)是黄芪的主要活性成分,研究发现APS能抑制肝癌HepG2细胞株的增殖,但其具体的作用机制暂不明确[3]。本研究旨在探究APS对于肝癌HepG2细胞铁死亡的调控机制作用,为临床上防治肝癌奠定理论基础。
1 材料与方法
1.1 细胞培养与APS处理
肝癌HepG2细胞(购自武汉普诺赛生物科技有限公司,货号:CL-0103)用含10%胎牛血清(美国Gibco公司,货号:10270-106)的DMEM(美国Gibco公司,货号:C12430500BT)培养基,在5%CO2、37℃的培养箱中培养。APS(货号:160901,质量分数大于98%)购自天津赛诺制药有限公司。采用对数期生长的肝癌HepG2细胞置于分别添加了50、100、200 mg/L APS的DMEM培养基中培养48 h后,再进行后续检测[4]。
1.2 CCK-8检测
取约3×104个肝癌HepG2细胞接种于96孔板,当细胞密度达到约70%时,采用不同浓度的APS药物处理48 h。而后,每孔中加入CCK-8试剂(日本DOJINDO公司,货号:CK04)避光培养4 h,检测每个孔在450 nm处的吸光值。每组实验重复3次。
1.3 铁离子检测
将接受不同浓度APS处理后的肝癌HepG2细胞裂解并离心,取离心后的上清液,与铁测定缓冲液混合反应30 min,再用铁探针(上海碧云天生物技术股份有限公司,货号:S1060)孵育1 h。最后在593 nm处测量吸光度,并计算总铁离子水平。每组实验重复3次。根据对照组的铁离子水平计算各组细胞内的相对铁离子水平并作图。
1.4 细胞内谷胱甘肽(GSH)、活性氧自由基(ROS)和脂质过氧化物水平的测定
将肝癌HepG2细胞接种于6孔板中培养,待细胞密度达到70%后,对各组细胞进行不同浓度的APS处理48 h。而后根据每个试剂盒说明书操作步骤,检测细胞内ROS(南京建成生物工程研究所,货号:E004-1-1)、GSH(南京建成生物工程研究所,货号:A005-1-2)和脂质过氧化物(南京建成生物工程研究所,货号:A106-1-2)活性。每组实验重复3次。APS处理组的结果均根据对照组进行均一化处理。
1.5 蛋白质印迹法(Western blot)检测
收集处理后的各组细胞,并用RIPA溶液裂解细胞,BCA法测定蛋白浓度。取等量蛋白用10%的SDS-PAGE胶分离,PVDF转膜、5%BSA室温封闭而后,进行一抗4℃过夜孵育孵育,所用一抗包含:Wnt(ab228626),蛋白谷胱甘肽过氧化物酶4(GPX4,ab125066),长链脂酰CoA合成酶4(ACSL4,ab155282),β-catenin(ab32572)和β-actin(ab8226)均购自上海Abcam公司。经过对应的二抗在37℃孵育1 h后,使用超敏ECL化学发光试剂盒(货号:P0018M,上海碧云天生物技术股份有限公司)显色,拍摄条带后用Image J分析相对灰度密度。每组实验重复3次。
1.6 统计学方法
采用GraphPad Prism 8软件进行数据分析,数据以 的统计结果表示,多组间比较采用方差分析。当P<0.05为差异有统计学意义。
2 结果
2.1 黄芪多糖对肝癌HepG2细胞增殖的影响
与对照组相比,黄芪多糖高、中、低剂量组均能降低肝癌HepG2细胞增殖(P<0.05),且呈剂量依赖性,见图1。
2.2 黄芪多糖对肝癌HepG2细胞GSH水平、ROS活力和脂质过氧化物水平的影响
与对照组相比,黄芪多糖高、中、低剂量组均能降低肝癌HepG2细胞GSH水平,并增加ROS和脂质过氧化物的积累(P<0.05),且呈剂量依赖性,见图2。
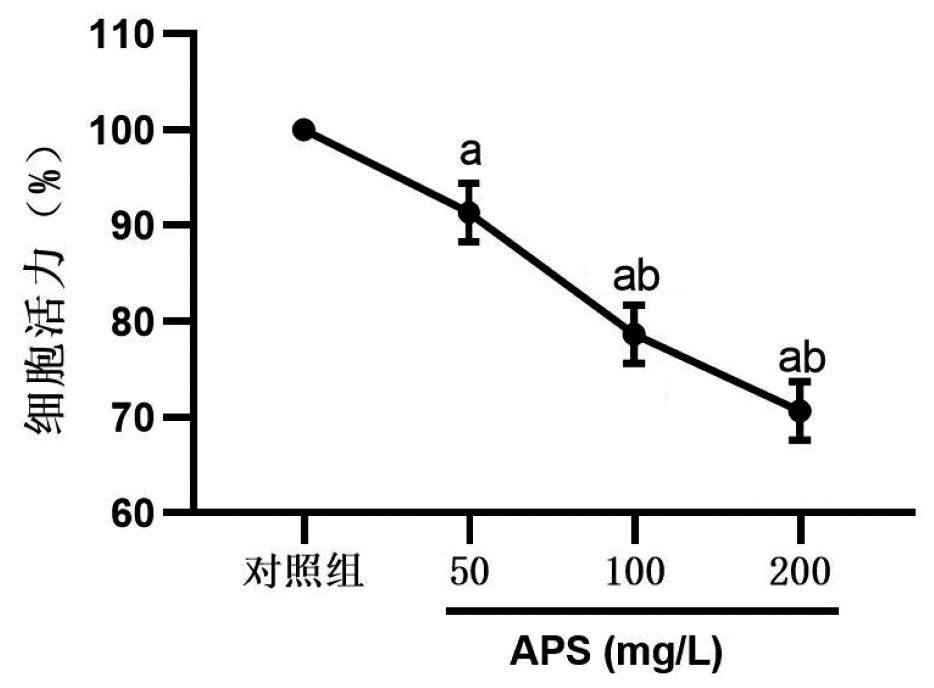
注:a与对照组相比,P<0.05;b与50 mg/L APS组相比,P<0.01
图1黄芪多糖对肝癌HepG2细胞增殖的影响

注:a与对照组相比,P<0.05;b与50 mg/L APS组相比,P<0.05
图2黄芪多糖对肝癌HepG2细胞GSH水平、ROS活力和脂质过氧化物水平的影响
2.3 黄芪多糖对肝癌HepG2细胞GPX4和ACSL4蛋白表达的影响
与对照组相比,黄芪多糖高、中、低剂量组均能抑制肝癌HepG2细胞GPX4蛋白表达,同时增强ACSL4蛋白表达 (P<0.05),且呈剂量依赖性,见图3。
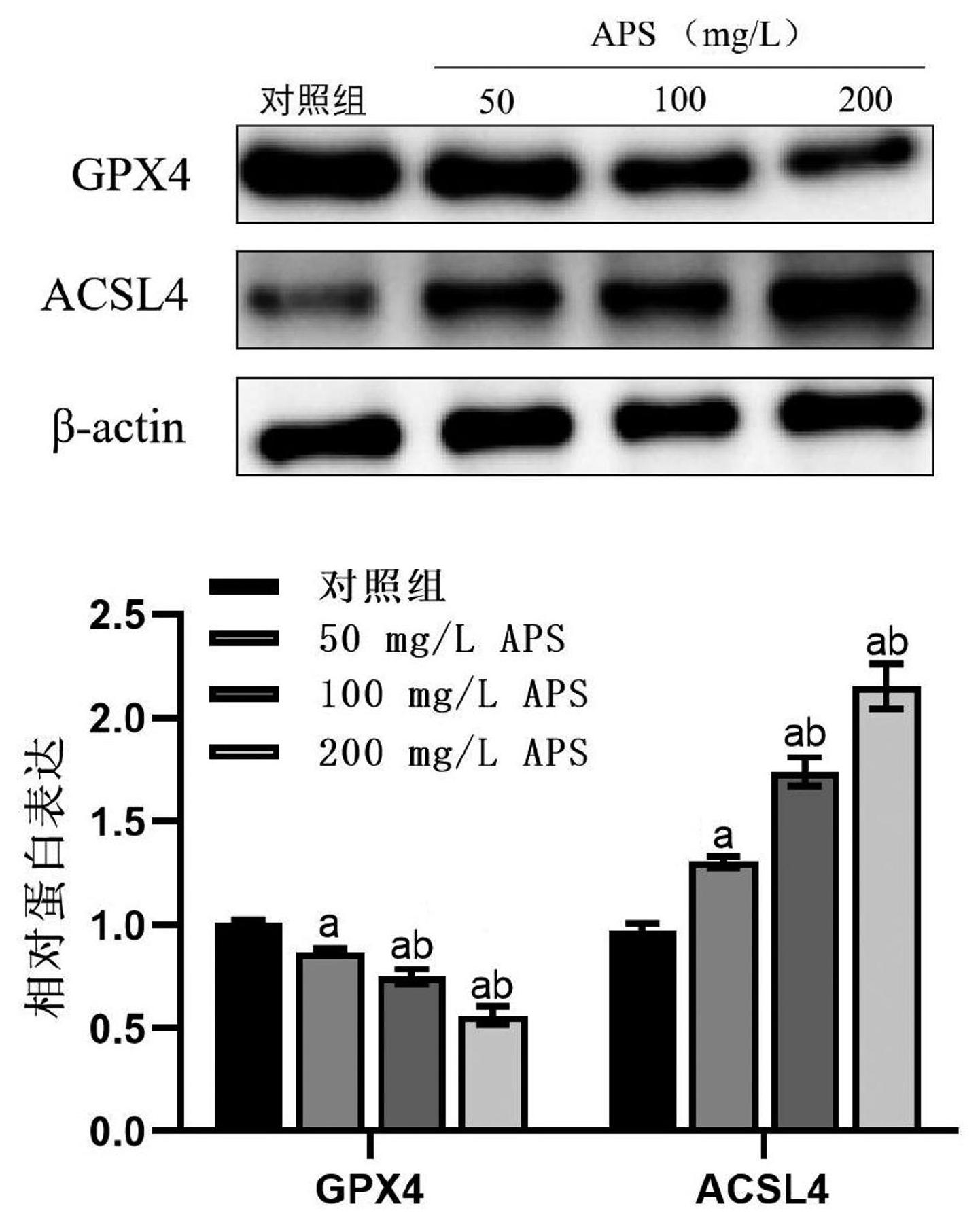
注:a与对照组相比,P<0.05;b与50 mg/L APS组相比,P<0.05
图3黄芪多糖对肝癌HepG2细胞GPX4和ACSL4蛋白表达的影响
2.4 黄芪多糖对肝癌HepG2细胞铁离子浓度的影响
与对照组相比,黄芪多糖高、中、低剂量组均能提高肝癌HepG2细胞的铁离子浓度(P<0.05),且呈剂量依赖性,见图4。
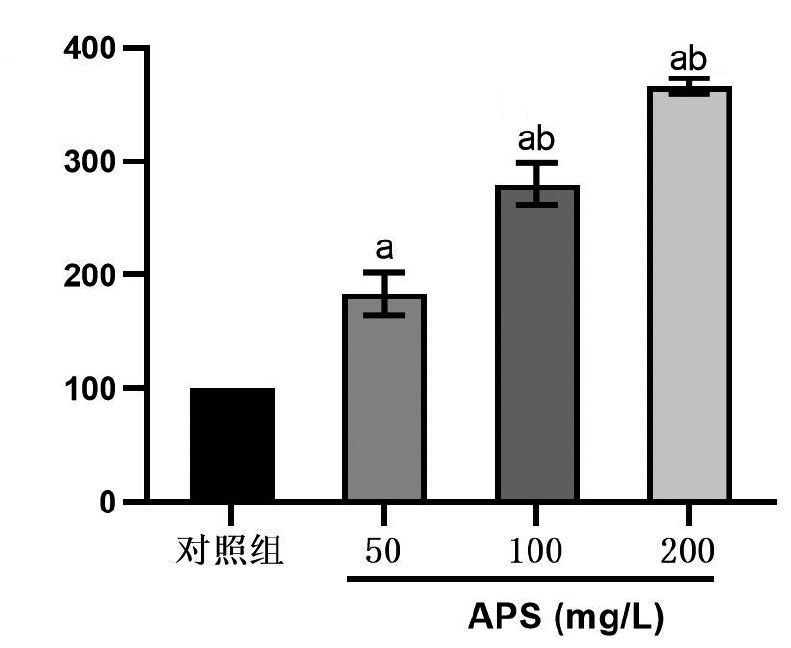
注:a与对照组相比,P<0.001;b与50 mg/L APS组相比,P<0.001
图4黄芪多糖对肝癌HepG2细胞铁离子浓度的影响
2.5 黄芪多糖对肝癌HepG2细胞内Wnt/β-catenin信号通路的影响
与对照组相比,黄芪多糖高、中、低剂量组均能有效减轻肝癌HepG2细胞的Wnt和β-catenin蛋白表达水平(P<0.05),且呈剂量依赖性,见图5。
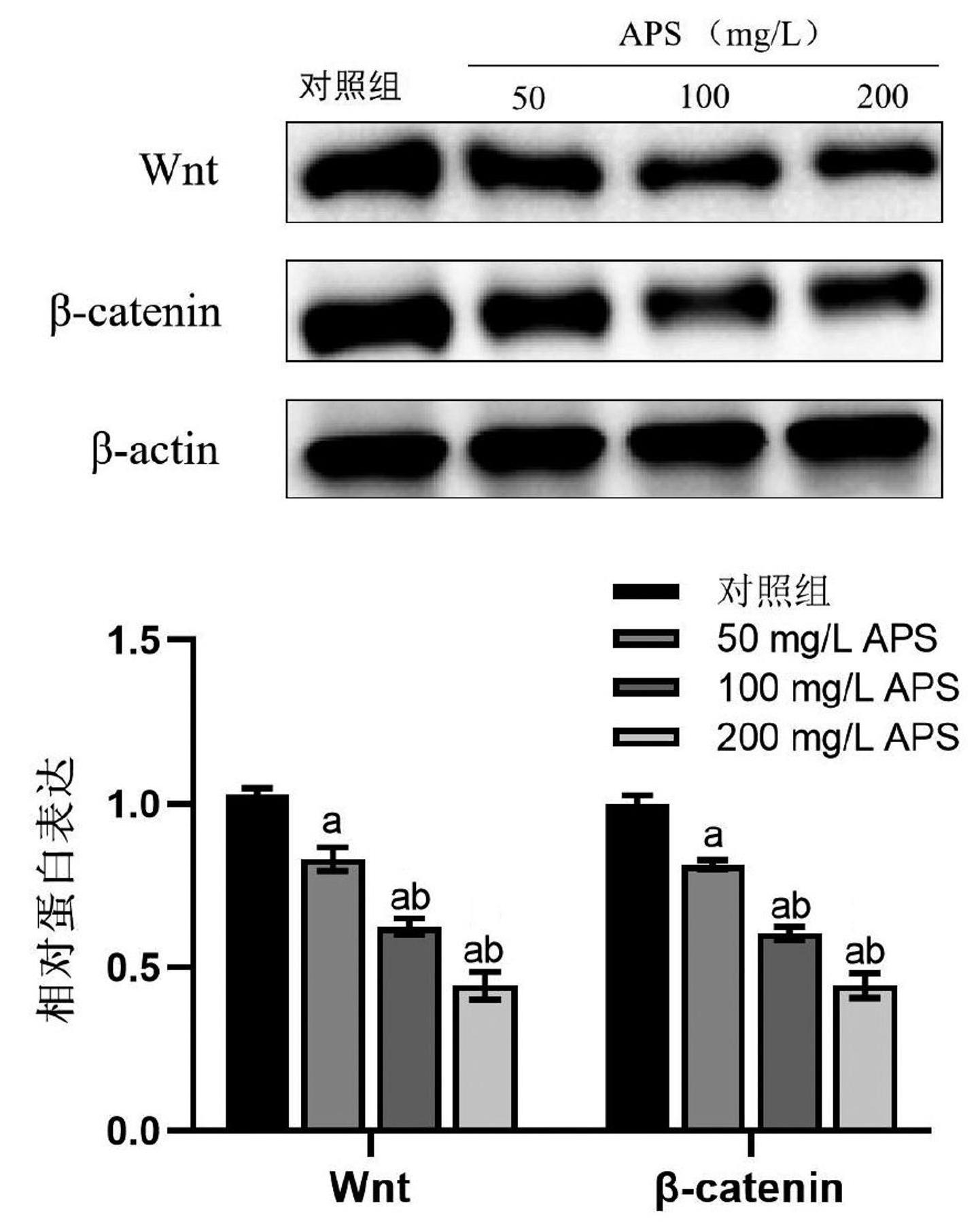
注:a与对照组相比,P<0.05;b与50 mg/L APS组相比,P<0.05
图5黄芪多糖对肝癌HepG2细胞内Wnt/β-catenin信号通路的影响
3 讨论
由于缺乏治疗肝癌的有效药物,肝癌患者的治疗一直是我国医疗健康产业面临的巨大难题。中药是我国的源远流长的宝贵资源,其物美价廉且药效好,在肝癌的综合治疗中发挥着重要的的作用。有文献曾经报道过,中药黄芪在治疗肝癌方面取得显著的临床疗效,尤其在改善肝癌患者的免疫功能方面[5]。根据《神农本草经》中记载:“黄芪,味甘微温,主痈疽久败创,排脓止痛,大风,痢疾,五痔,鼠瘘,补虚,小儿百病。”黄芪具有健脾益气固表、脱毒生肌、利尿排脓等作用[6]。APS是黄芪的主要活性成分,可以通过调控肿瘤微环境及免疫系统、调节肿瘤细胞生长周期等多种方式发挥抗癌、抗炎及免疫调节、抗氧化、抗细胞凋亡、代谢调节等作用[7]。并且,有相关研究报道,APS能通过影响细胞周期使之阻滞于G1期,诱导细胞凋亡从而抑制肝癌细胞的增殖[3]。本研究也发现,APS能够抑制肝癌细胞增殖,并随着APS的浓度升高,细胞增殖的抑制能力逐渐增强,对于其抑制机制的原理,需要进一步的实验进行验证。
铁死亡是一种新的细胞程序性死亡的方式,其具体的作用机制是细胞内过多的游离铁诱导脂类发生过氧化反应,生成脂质过氧化物超过细胞内抗氧化系统的负荷,进而诱导细胞发生死亡[8]。GPX4是一种硒代半胱氨酸酶,是抗氧化反应和铁死亡的中心调控因子[9]。GSH是重要的抗氧化剂和自由基清除剂,能够辅助GPX4还原ROS和氧化脂类。当GSH减少时,GPX4活性降低,氧化反应占据主导地位,ROS和脂类过氧化物的积累,最终导致细胞死亡[10]。因此,其主要特征是Fe离子浓度升高、GPX4活性降低、GSH的消耗、ROS及脂质过氧化物的大量积累。近期大量研究发现,从中药中提取的活性物质例如葫芦素B和二氢青蒿等都能通过增强肝癌细胞的铁死亡抑制肝癌细胞的增殖[11-12]。相似地,本研究发现APS能够降低肝癌HepG2细胞内GSH的水平,增加ROS和脂质过氧化物的积累,同时提高铁离子浓度,表明APS能够增强细胞铁死亡水平,进而达到抑制肝癌细胞增殖的结果。除了GXP4,ACSL4可以促进长链不饱和脂肪酸活化,在脂肪酸代谢中发挥重要作用,当ACSL4缺失时,可导致长链不饱和脂肪酸被氧化,诱导铁死亡[13]。因此,ACSL4在铁死亡的过程中表达上调,是铁死亡重要的标志物之一[14]。本研究也发现,APS处理后,肝癌细胞中的GXP4表达下调,ACSL4表达上调,进一步证实了APS处理能促进肝癌HepG2细胞铁死亡,进而抑制肝癌细胞的增殖。
Wnt/β-catenin信号通路已被报道参与肿瘤细胞的增殖、迁移和侵袭等过程,是癌症中最经典的通路之一。不仅如此,Yin等[15]研究发现circAFF1通过靶向miR-140-5p调节Wnt/β-catenin信号通路诱导神经元铁死亡。Wang等[16]证明激活Wnt/β-catenin信号通路能减弱胃癌细胞脂质ROS的产生,进而抑制胃癌细胞铁死亡,促进胃癌细胞的增殖。近年来,许多研究报道中药有效成分可通过该通路发挥抗肝癌作用[17]。丁娜等[18]发现青蒿琥酯通过抑制Wnt/β-catenin信号通路抑制卵巢癌细胞增殖,促进铁死亡。同样地,本研究发现APS在促进肝癌HepG2细胞铁死亡,抑制细胞增殖的的同时,还能抑制Wnt和β-catenin蛋白的表达,抑制Wnt/β-catenin信号通路的激活。基于此,APS对肝癌HepG2细胞增殖的抑制作用可能是通过抑制Wnt/β-catenin信号通路促进铁死亡介导。本研究首次验证APS对于肝癌细胞的抑制作用是通过促进细胞铁死亡介导的,可能与Wnt/β-catenin信号通路的抑制有关,后期可以通过Wnt/β-catenin信号通路抑制剂进一步验证,并且可以通过增加更详细的动物实验进行多方位的验证。
综上所述,APS通过增强ROS和脂质过氧化物的积累增强铁死亡,抑制肝癌细胞的增殖,这一过程可能与Wnt/β-catenin信号通路的抑制有关,有望为将来APS用于临床上肝癌患者的防治奠定理论基础。





