摘要
目的:探索超声在腹腔间室综合征(ACS)患者管理中的作用。方法:选取2023年7月—2024年6月我院重症医学科收治的30例ACS患者为研究对象,接受超声作为ACS管理的辅助工具。结果:30例ACS患者的年龄为(60.0±14.6)岁,男性占70%,平均体质量指数(BMI)为(25.0±2.4)kg/m2,80%的ACS患者合并低血压需应用升压药物,ACS最常见的原因是腹腔感染导致的脓毒症和肠梗阻,分别占40%和20%。连续治疗5 d,平均腹腔内压力(IAP)从入院时(23±2.3)mmHg,下降至第5天(13±2.2)mmHg(P<0.001)。患者第1天平均APP为(62±5.5)mmHg,治疗第5天升为(90±5.4)mmHg(P<0.001),尿量是从第4天开始明显增加,且伴随肾动脉阻力指数下降至0.65±0.06(P<0.001)。超声提示在第1天出现肠道功能障碍的患者有10例,占总患者的33.3%,经胃肠减压、灌肠等处理后,第5天仅有1例患者仍存在肠道功能障碍;超声可以识别肠腔内容物,进一步指导患者减压或灌肠,同时对于8例合并腹腔积液的患者,进行了超声引导穿刺术。结论:在ACS患者治疗管理中,相比传统应用腹腔灌注压(APP)评估腹腔内器官的灌注,经超声测量的肾动脉阻力指数可以更加敏感地评估肾脏灌注的;超声在评估肠道功能,识别肠腔内容物,指导进行减压、灌肠,引导腹腔积液引流管的放置均有优势。
Abstract
Objective To explore the role of ultrasonography in the management of patients with abdominal compartment syndrome (ACS). Methods Thirty patients diagnosed with ACS were included as research subjects, employing ultrasonography as an auxiliary tool for ACS management. Results The study encompassed 30 patients, with an average age of (60.0±14.6) years, 70% of whom were male, and an average BMI of (25.0±2.4)kg/m2. Eighty percent of the patients with ACS required vasopressor support due to hypotension, with the most common causes of ACS being sepsis due to intra-abdominal infection, and intestinal obstruction, accounting for 40% and 20% respectively. After five consecutive days of treatment, the average intra-abdominal pressure (IAP) decreased from (23±2.3)mmHg at admission to (13±2.2)mmHg on the fifth day. The patient's average APP on the first day was (62±5.5)mmHg, which rose to (90±5.4)mmHg by the fifth day of treatment. However, a significant increase in urine output was observed starting from the third day, accompanied by a decrease in the renal artery resistance index to 0.65±0.06. Ultrasound indicated intestinal dysfunction in 10 patients (33.3% of the total) on the first day, which was reduced to one patient by the fifth day following gastrointestinal decompression and enema treatments; ultrasonography could identify intestinal contents, further guiding decompression or enema procedures. Additionally, for eight patients with concurrent ascites, ultrasound-guided paracentesis was performed. Conclusion In the treatment and management of patients with ACS, compared to the traditional application of APP for assessing perfusion of intra-abdominal organs, the renal artery resistance index measured by ultrasonography can more sensitively evaluate renal perfusion. Ultrasound has advantages in evaluating intestinal function, identifying contents within the intestinal lumen, guiding decompression and enema administration, and guiding the placement of abdominal fluid drainage tubes.
腹腔内高压(intra-abdominal hypertension,IAH)和腹腔间室综合征(abdominal compartment syndrome,ACS)是影响危重症患者发病率及死亡率的确定因素[1],并且IAH/ACS在入住重症监护室(intensive care unit,ICU)的患者中普遍存在[2]。世界腹腔间室综合征学会(world society of the ACS,WSACS)于2013年发布的IAH/ACS管理指南主要是基于定期腹腔内压力(intra-abdominal pressure,IAP)的测量值制定的[3]。ACS被定义为持续IAP>20 mmHg合并新发的器官功能障碍或衰竭[4]。IAP的测量分为直接测量(即应用穿刺针穿刺腹腔、腹膜透析管路或腹腔镜进而测量压力)和间接测量(即通过球囊导管测量膀胱、胃、结肠或子宫腔内的压力)。直接测量为有创性方法,临床应用受限;通过测量膀胱内压力的间接测量IAP的方法具有实施简单、成本最小的特点,在全球得到了最广泛的应用,并且膀胱压与IAP有良好的相关性,连续监测膀胱压是早期发现ACS的“金标准”[5]。但该方法低估了患者病情动态变化的实时性和病因的复杂性,临床推广应用不佳[6]。超声作为重症专业及相关医师的多维信息获取手段,是重症管理过程中必须掌握的技能[7-8]。本研究旨在制定超声对于ACS患者管理的新流程,对ACS患者实施可视化、个体化管理,从而早期明确病因,早期干预,改善预后。
1 资料与方法
1.1 一般资料
应用前瞻性观察性研究方法,选取2023年7月—2024年6月我院重症医学科收治的30例ACS患者为研究对象。纳入标准:1)最少在ICU住院5 d;2)年龄≥18岁;3)气管插管机械通气患者充分镇静[Richmond躁动-镇静评分(RASS)为-4分或-5分];4)能够仰卧位进行所有测量;5)没有腹部肌肉的收缩。排除标准:5 d内死亡,入ICU后5 d内拔除气管插管或从ICU转出,或初始IAP<20 mmHg。本研究经本院伦理委员会审批通过(审批号:2023DZX11)。患者及家属同意本研究并签署知情同意书。
1.2 IAP的测量
根据2013年WSACS指南常规测量IAP。患者仰卧位,无菌操作经尿道膀胱置入插入Forley's尿管,放松腹壁肌肉,排空膀胱后,将25 mL的0.9%氯化钠注射液(温度为37~40℃)注入尿管内,连接测压管,以患者髂嵴与腋中线交点为零点,排尽空气使测压管与大气相通,当测压管的液面有轻微波动而不再下降时,患者呼气末测压管内液面凹面所对的刻度数字为腹内压;考虑膀胱充盈性,每隔1 min测量1次,重复测量2次,取平均值。
1.3 临床指标的获取
记录每个患者的临床资料、初始生命体征、入院IAP、鼻胃管成功留置人数、血液净化治疗天数、机械通气时间,连续5 d监测IAP、液体平衡、尿量、肾血流半定量评分、肾动脉阻力指数(resistance index,RI)等指标。计算入院腹腔灌注压(abdominal perfusion pressure,APP)=平均动脉压(mean arterial pressure,MAP)-IAP。
1.4 超声检查
所有入组患者由同一名训练有素的重症医师在患者入院后的5 d连续使用Versana Active超声诊断仪(GE公司)进行超声评估策略并指导干预,并由另外一名训练有素的重症医师进行超声评估的质量控制。具体操作方法如下:1)超声引导留置鼻胃管。采用“4点法”超声检查方案:从患者左侧颈部进行超声检查以观察食管(图1a),行上腹超声检查以确认通过食管胃交界处的情况(图1b),确认在胃窦的位置(图1c),进行胃底超声检查(图1d),并拍摄X线片最终确认鼻胃管的位置。2)超声评估肠道功能:探头放置位置(见图2),评估小肠及结肠的宽度、厚度、运动度(表1)。如出现肠功能紊乱应减少肠内营养甚至停用并给予减压、灌肠。3)超声发现腹腔内游离液体并引导穿刺。4)超声评估肾血流半定量评分:患者取仰卧位,超声探头置于腋中线或肋弓下缘,分别通过肝脏右叶下部及脾脏寻找并显示右侧和左侧肾脏。在标准切面的基础上,打开彩色多普勒,将取样框调整合适大小至于肾脏,显示肾血流。根据彩色多普勒血流显示情况,进行半定量评分(表2)。5)超声评估肾动脉阻力指数:肾脏切面的基础上,打开彩色多普勒采样框至肾脏区域,调整合适大小后进行血流显像,在彩色多普勒成像(CDFI)基础上结合脉冲多普勒技术可对叶间动脉或弓状动脉的血流采集获取3个连续相似的波形,测量收缩期峰流速和舒张期最小流速,RI=(收缩期血流速度峰值-舒张末期血流速度)/收缩期血流速度峰值,重复测量3次,取平均值。
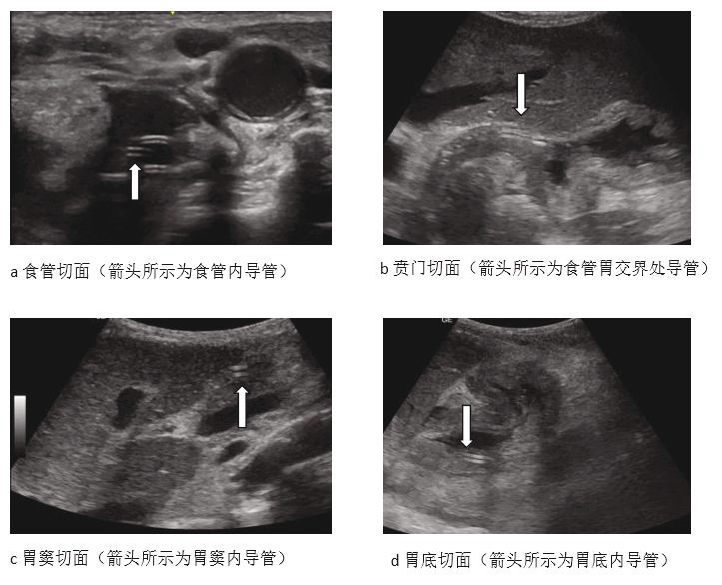
图1“4点法”超声检查方案行超声引导留置鼻胃管
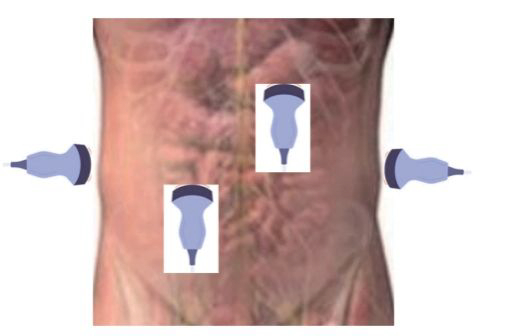
图2超声评估肠道功能的探头放置位置(空肠、回肠、左半结肠、右半结肠)
表1肠道功能判定标准

表2肾血流半定量评分标准

1.5 统计学方法
使用SPSS 21.0统计软件进行分析,计数资料以均数±标准差()表示,多组间比较采用重复测量方差分析(ANOVA),两组间比较采用样本t检验;计数资料比较使用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 患者基本资料及入院主要病因
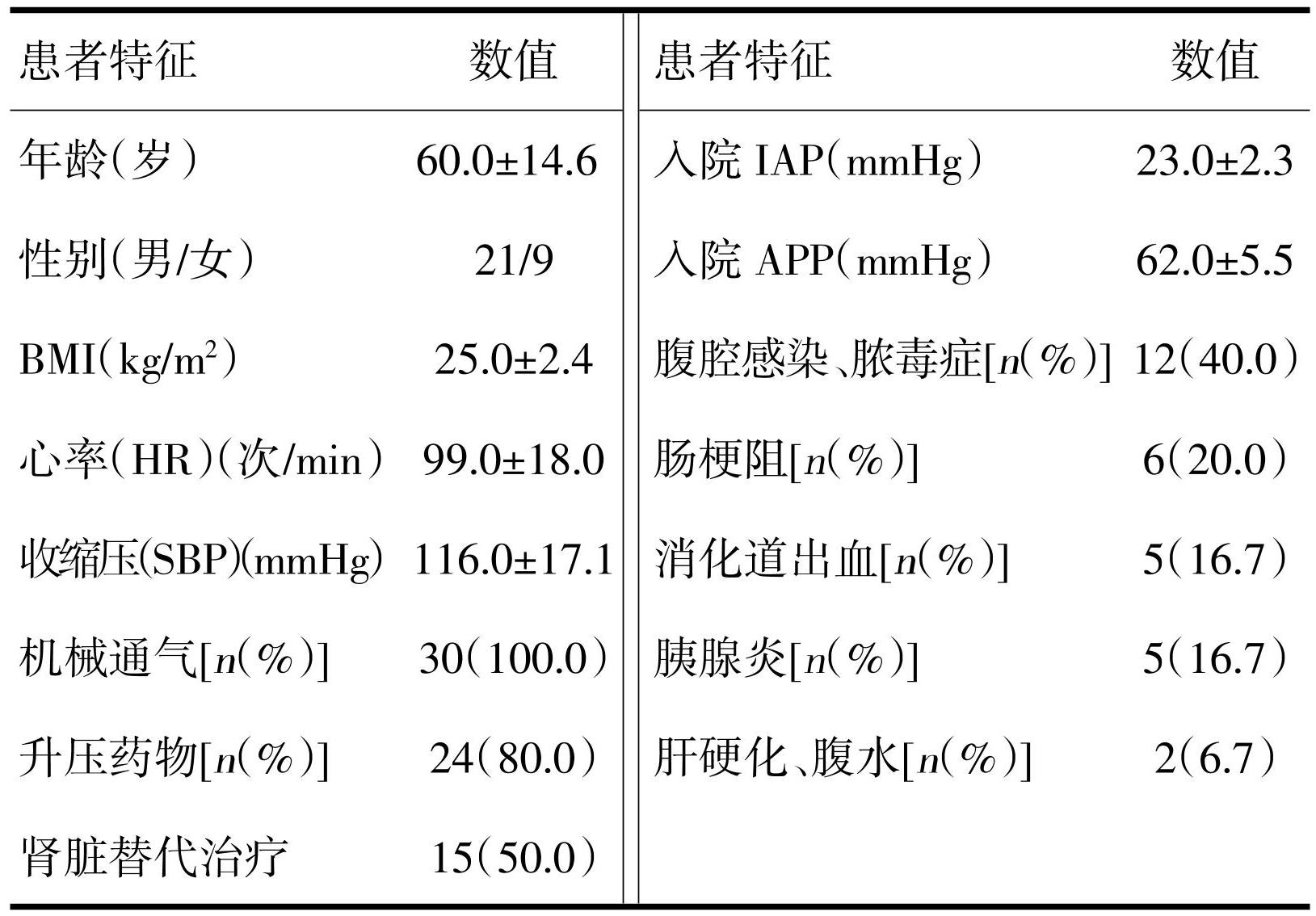
本研究纳入的30例患者的平均年龄为(60.0±14.6)岁,男性占70%,平均体重指数(BMI)为(25.0±2.4)kg/m2,80%的ACS患者合并低血压需应用升压药物。ACS最常见的原因是腹腔感染导致的脓毒症和肠梗阻,分别占40%和20%。见表3。
表3患者入院基本资料及入院主要病因
2.2 30例ACS患者治疗连续5 d的监测数据
30例ACS患者入院时的平均IAP为(23±2.3)mmHg,经治疗后第5天,平均IAP下降至(13±2.2)mmHg(P<0.001),由于临床管理后所有患者腹腔内压力均有所下降,均不需行剖腹手术干预。患者第1天平均APP为(62±5.5)mmHg,治疗后第5天上升至(90±5.4)mmHg(P<0.001),但尿量是从第4天开始明显增加,且伴随肾动脉阻力指数下降至0.65±0.06(P<0.001)。超声可通过监测肠管宽度、肠壁厚度及肠道活动度评估肠道功能,在第1天超声检测出肠道功能障碍患者10例,占33.3%,经胃肠减压、灌肠等处理后,第5天仅有1例患者仍存在肠道功能障碍。超声可以识别肠腔内容物,指导患者减压或灌肠进而减低IAP,但同时还发现灌肠治疗在第1、3、5天分别有90%、61%、36%的患者肠道排空不完全。超声显示有16例ACS患者存在腹腔积液,其中8例进行了超声引导穿刺术,见表4。
3 讨论
腹腔内高压及腹腔间室综合征在重症患者中的发生并不鲜见,文献报道在ICU中其发病率分别为27.7%和2.7%;在创伤后入住ICU的患者中,ACS的发病率为4.2%~14%[9]。腹内高压可引起器官组织低灌注,甚至发展至腹腔间室综合征,导致出现多器官和系统功能障碍,给救治带来很大的挑战。腹腔是一个封闭的空间,腹腔容积增加和腹壁顺应性减退均可导致腹内压增高,临床常见的原因为出血、感染、肿瘤和液体过负荷等[10]。本研究显示ACS最常见的原因是腹腔感染导致的脓毒症和肠梗阻,分别占病因的40%和20%。
表430例ACS患者治疗连续5 d的监测数据
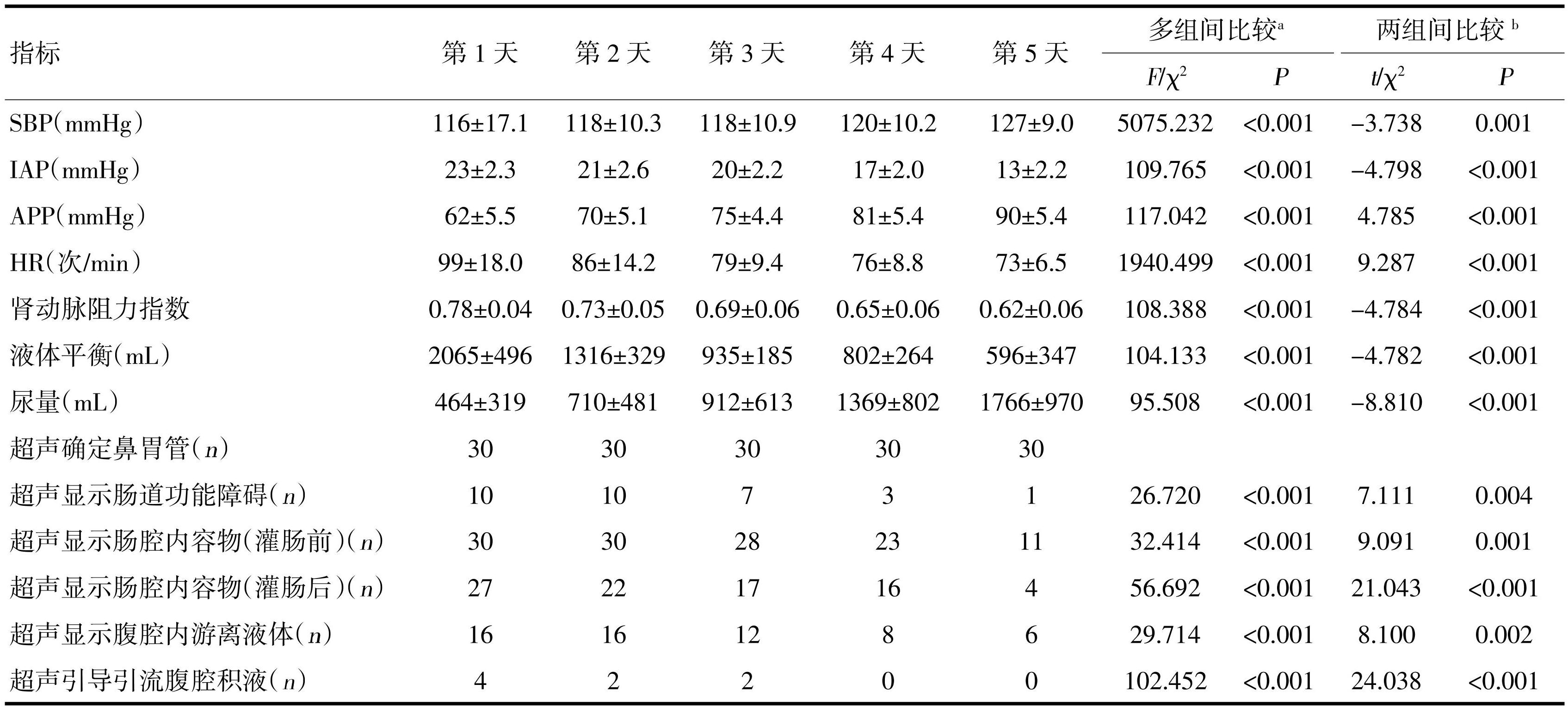
注:a指第1~5天比较;b指第1天和第5天两组间比较
尽管IAP值一直被认为是管理IAH/ACS的最重要因素,但在临床实践中个体患者需要考虑的因素包括IAP测量方法和测量IAP的环境,IAP的预期基线值,IAP随时间的演变,以及患者已经暴露于IAH/ACS的持续时间。针对IAH/ACS患者的最佳治疗选择应考虑三个关键因素:1)测量的IAP值(或IAP增加的程度及幅度);2)器官功能障碍(或IAP的增加对器官功能产生的影响);3)潜在疾病的性质与病程。使用这种“IAP值、器官功能障碍、潜在疾病性质与病程”的相互作用的三角治疗模式被充分认识,除了测量的IAP值之外,其他两个因素也很重要[6]。
肥胖作为影响腹壁顺应性的常见原因,加剧了其他因素导致IAP升高的结果,并且降低了IAH发展至ACS 所需的阈值[11]。肥胖的发病率正在逐年上升,据估计,到2030年,肥胖症的发病率将占全世界成年人口的38%[12]。此外,研究表明,IAP的升高与肥胖以及与肥胖相关的疾病相关,如高血压、胃食管反流症和阻塞性睡眠呼吸暂停综合征[12]。因此监测肥胖患者的IAP非常重要。而IAP基线存在个体差异,尤其肥胖患者具有较高的IAP基线值,在某些情况下可能高于IAH阈值[13]。De Keulenaer等[14]研究发现,体质量正常人的IAP约为5~6 mmHg,而肥胖患者的IAP则高得多,其值可以高于12 mmHg,病态肥胖患者甚至高于14 mmHg。这与本研究纳入的IAH患者的BMI为(25±2.4)kg/m2相似,并且研究组患者第5天平均尿量明显增多至(1766±970)mL,其平均腹腔内压力仍为(13±2.2)mmHg。
多器官功能障碍是ACS的主要特征之一。急性肾损伤(AKI)是最为常见的受累器官[15]。在ACS患者中,AKI通常表现为无尿和需要肾脏替代治疗(RRT)[16]。本研究中有15例患者出现AKI并行RRT,占本组研究人数的50%。
根据WSACS的建议,APP=MAP-IAP,与MAP或腹内压比较,APP是更好的内脏灌注指标[17]。Gül等[18]研究结果表明:APP≥60 mmHg是合适的复苏目标。但是无证据表明,在上述公式适用于高剂量的血管活性药物的患者。血管活性药物的使用及其对收缩压的影响可能掩盖潜在的腹腔内灌流不足,这是由血管活性剂引起的血管收缩的结果。因此,相对正常的APP可能不能准确反映腹腔灌注。Cheatham等[17]认为当血管活性药物使用情况下,测量APP是不可靠的。Yin等[19]研究证实中国重症超声研究组(CCUSG)提出的超声引导AKI的“ABCDE”方案采用二维肾血流分布、肾动静脉血流谱、肾阻力指数(RRI)、等综合评价肾脏灌注情况,有利于指导治疗。肾动脉阻力指数是通过超声多普勒对血流速度进行一段时间连续检测后间接获得的指标,在一定范围内可以直接反映肾血管阻力情况及微循环灌注变化,同时RRI还受到腹腔内不断改变的压力影响。Kajal等[20]研究表明,术中RRI增加是患者术后发生急性肾损伤的独立预测因子。本研究ACS患者第1天平均APP为(62±5.5)mmHg,伴随治疗至第5天上升为(90±5.4)mmHg,但尿量增加是从第3天开始明显增加,且伴随肾动脉阻力指数下降至0.65±0.06,提示APP在评估肾脏灌注存在滞后性,应用肾动脉阻力指数更加敏感。
IAH/ACS管理中需要考虑的第三个因素是IAP升高的病因,这有利于选择最佳的治疗方案。IAH/ACS的多种风险因素,但它们可能主要分为三类:腹内容量增加、腹部顺应性下降以及两者的结合[21]。这可能是由腹腔中消化道管腔内或管腔外容积增加引起的。本研究证实超声可通过监测肠管宽度、肠壁厚度及肠道活动度评估肠道功能,早期识别肠道功能障碍患者,同时超声能很好的识别肠腔内容物,并指导患者进行减压或灌肠,减少了患者过度的床旁X线的暴露,同时可以引导腹腔积液引流管的放置从而减低IAP。
综上所述,在ACS患者治疗管理中,相比传统的评估腹腔内器官灌注的APP,超声测量的肾动脉阻力指数可以更加敏感的指导肾脏灌注的评估;超声在评估肠道功能,识别肠腔内容物,指导进行减压、灌肠,引导腹腔积液引流管的放置均有其优势。本研究的主要局限性为小样本单中心观察性研究,下一步需扩大样本量,并行随机对照试验以评估临床结果。






