摘要
目的:基于环磷酸腺苷反应元件结合蛋白3(CREB3)对高尔基体的应激作用研究电针刺在减轻小鼠内毒素急性肺损伤中的作用机制。方法:选取SPF级健康雄性C57BL/6J小鼠24只,7~8周龄,体质量25~30g ,随机分成4组:空白对照组(WT组)内毒素相关性急性肺损伤模型组(LPS组)模型+电针刺组(EA+LPS 组)模型+电针刺激非穴位组(SEA+LPS 组),每组6只。EA+LPS 组于模型制备前5天采用电针刺小鼠双侧足三里(ST36)和双侧肺俞穴(BL13),SEA+LPS组用同样的方法刺激远端非穴位处。LPS 组、EA+LPS 组和SEA+LPS 组腹腔注射脂多糖(LPS)12mg/kg ,WT组给予等容量生理盐水。注射LPS 或生理盐水12h后,取血并分离血清检测肿瘤坏死因子(TNF)-α、白细胞介素(IL)-1β 和 IL-6 浓度,取肺组织并进行病理损伤评分,免疫荧光染色观察高尔基体形态,检测CREB3蛋白的表达水平及Golgin97、GRASP65和GOLPH3高尔基体应激相关指标的蛋白表达水平。结果:与LPS组比较,EA+LPS 组肺损伤减轻,显微镜下高尔基体损伤程度减轻,血清TNF-α、IL-1、IL-6含量降低(P<0.05),肺组织CREB3 蛋白表达水平下调,高尔基体应激相关蛋白Golgin97、GRASP65 表达上调,而GOLPH3表达下调(P<0.05),但SEA+LPS 组上述各指标与LPS组差异无统计学意义(P>0.05);CREB3敲除小鼠可逆转电针刺对高尔基体应激及脓毒症肺损伤的治疗效果。结论:电针刺激双侧足三里和双侧肺俞穴减轻小鼠内毒素急性肺损伤的作用机制可能与CREB3介导高尔基体应激有关。
Abstract
Objective To investigate the role of cAMP response element -binding protein 3 (CREB3) in alleviating Golgi stress in endotoxin -induced acute lung injury in mice through electroacupuncture (EA).Methods 24 healthy male SPF-grade C57BL/6J mice, aged 7-8 weeks and weighing 25~30g . were randomly divided into 4 groups (n=6): WT operation group (WT group), endotoxin-induced acute lung injury model group (LPS group), model+electroacupuncture group (EA +LPS group), and model+electroacupuncture at non-acupoint group(SEA +LPS group). The EA+LPS group received electroacupuncture at bilateral Zusanli and Feishu acupoints for 5 days prior to model induction, while the SEA+LPS group was stimulated at distant non-acupoints using the same method. The LPS group, EA+LPS group, and SEA+LPS group received intraperitoneal injections of lipopolysaccharide (LPS) at a dose of 12mg/kg , while the WT group was given an equivalent volume of normal saline. 12 hours afer the injection of LPS or normal saline, blood samples were collected, and serum was separated to measure the concentrations of tumor necrosis factor (TNF)-α, Interleukin (IL)-1β, and IL-6. Lung tissues were collected for pathological injury scoring, immunofluorescence staining to observe Golgi morphology, and detection of CREB3 protein expression levels, as well as the protein expression of Golgi stress -related markers Golgin97, GRASP65, and GOLPH3. Results Compared with the LPS group, the EA+LPS group showed a decrease in lung injury scores, reduced Golgi damage under the microscope, and lower concentrations of serum TNF -α, serum IL-1, and serum IL-6 (P<0.05). Additionally, the expression levels of CREB3 protein in lung tissue were downregulated, while the expression of Golgi stress -related proteins Golgin97 and GRASP65 were upregulated, and GOLPH3 expression was downregulated (P<0.05). However, in the SEA +LPS group, there were no statistically significant differences in these indicators (P>0.05). CREB3 knockout mice can reverse the therapeutic effects of electroacupuncture on Golgi apparatus stress and sepsis induced lung injury. Conclusion The mechanism by which CREB3 mediates the alleviation of endotoxin -induced acute lung injury in mice through electroacupuncture at Zusanli and Feishu acupoints may be related to Golgi stress.
Keywords
内毒素急性肺损伤发病率高且发病机制复杂,是急危重症高病死率的主要原因[1]。脂多糖(LPS)可引引起过度炎症,刺激细胞因子、活性氧的大量释放,导致多器官功能障碍,其中以急性肺损伤最常见且较严重[2-3]。细胞器功能障碍是内毒素急性肺损伤发病的重要机制之一[4]。本研究团队前期研究已证实,调节高尔基体应激可减轻内毒素诱导的急性肺损伤[5]。高尔基体可以作为一个信号中枢来整合和传导应力[6-7],各种刺激直接影响高尔基复合体的内稳态,导致“高尔基应激”,通常表现为高尔基体形状和功能的破坏[8-9]。炎症因子被认为是高尔基体应激的下游效应物,高尔基体应激参与炎症反应并介导炎症体的聚集[10-11]。环磷酸腺苷反应元件结合蛋白3(CREB3)属于碱性亮氨酸拉链转录因子(bZIP)家族。有研究发现,调控CREB3 转录因子及下游靶基因生长素反应因子基因 4(ARF4)的表达水平对控制原发性和转移性肺癌的发生发展有重要意义[12]。干预高尔基应激反应有助于减轻过度的炎症反应和对抗细菌感染,表明干预高尔基应激反应是预防和治疗内毒素急性肺损伤的一个有前途的研究领域。目前临床上调节全身性炎症的药物或方法在治疗内毒素急性肺损伤中的作用有限[13-14]。电针刺激治疗(EA)以传统针灸为基础,通过改变电刺激强度、频率、波形脉冲间隔等参数而进行行针治疗[15]。作为重要的辅助性治疗手段,目前临床上已将电针刺用于治疗包括肺部炎症损伤在内的多种疾病,但其作用机制尚未阐明。有研究证实,EA具有显著的抗炎作用,EA 可通过减少肺部炎症和维护细胞稳态以达到肺损伤时对肺脏的保护作用[13,16]。本研究团队已证实电针可显著减轻脂多糖(LPS)诱导的炎症反应和肺损伤,但其具体机制尚未完全阐明[17-18]。本研究拟通过研究CREB3在高尔基体应激中的作用,探讨电针刺减轻内毒素诱发小鼠急性肺损伤的作用机制。
1 材料与方法
1.1 实验动物及分组
选取 7~8 周龄 SPF 级健康雄性C57BL/6J小鼠24只,体质量25~30g,由天津市南开医院动物实验中心提供,于自然昼夜交替、23℃ 室温下饲养,自由进食水。实验前禁食24h,自由饮水,制备内毒素诱导急性肺损伤模型。随机分为4组:空白对照组(WT组)、内毒素相关性急性肺损伤模型组(LPS组)、模型+电针刺组(EA+LPS 组)、模型+电针刺激非穴位组(SEA+LPS 组),每组6 只。在C57BL/6背景上的CREB3条件敲小鼠(CREB3-KO)购自北京百奥赛图有限公司。为了评估CREB3对LPS诱导的急性肺损伤的影响,准备他莫昔非诱导的条件敲除小鼠6只,并进一步设置对照组:模型+电针刺组(LPS+EA 组)、敲除鼠模型+电针刺组(CREB3−KO+LPS+EA 组),每组6只。本研究获天津市南开医院动物伦理委员会批准(编号:NKYY-DWLL-2022-087)。
1.2 动物模型制备
参照中国针灸学会实验针灸研究会制定的《动物针灸穴位图谱》,EA+LPS 组选取小鼠双侧足三里穴(ST36)和肺俞穴(BL13),将小鼠置于自制固定管中,暴露针刺部位,常规备皮消毒,使用直径0.1mm 的一次性无菌针灸针,直刺进针约3~5mm。采用SDZ-Ⅲ型电针刺激仪,在固定时间段每天进行电刺激30min/次,模型制备前5d及模型制备过程中行电针处理。针刺参数为:疏密波,频率2Hz,刺激电流4~5 mA,刺激强度以小鼠肢体出现轻微颤动为宜。SEA+LPS 组使用同型号针,通过刺激非穴位进行对照治疗。给予LPS前12h 禁食,制备内毒素诱发急性肺损伤模型。称取每只实验小鼠的体质量,并计算所需LPS 溶液的给药剂量(12mg/kg),使用一次性注射器抽取备好的要用药量。固定小鼠,缓慢注射相应剂量的LPS或等量PBS于小鼠腹腔内,注射后放回其熟悉的笼子继续饲养。每隔2h记录小鼠体质量及体温变化。
1.3 标本采集与保存
注射LPS后12h,小鼠接受异氟烷麻醉。采用内毗取血法取血于促凝管中;静置30min 后,以3500r/min 离心5min,吸取分离的血清置于冻存管中,−80℃保存待用。安乐死法处死小鼠后,摘取肺组织,右肺叶切小块置于戊二醛中,左肺叶置于多聚甲醛中,其余肺组织置于液氮罐中,速冻后于−80℃低温冰箱保存,根据后续实验需要进行相应处理。
1.4 检测指标及检测方法
1.4.1 SDS-聚丙烯酰胺凝胶电泳检测CREB3、GRASP65、Golgin97、GOLPH3蛋白水平
首先用RIPA缓冲液从肺组织中提取蛋白质,使用BCA 蛋白检测试剂盒检测蛋白浓度。等量的蛋白质加样至10% SDS-PAGE凝胶,后转移到PVDF膜上。用5%脱脂奶粉在TBST中封闭1h,并在4℃下孵育过夜,一抗β-actin(1:2000稀释,abcam)、CREB3(1:1000稀释,Santa)、GRASP65(1:1000稀释,Santa)、Golgin97(1:1000稀释,CST)、GOLPH3(1:1000 稀释,Proteintech)。然后用TBST洗涤3次,每次10min。洗净后,辣根过氧化物酶偶联山羊抗小鼠免疫球蛋白G(1:10000稀释,Santa)。用增强化学发光法使条带显影,以目的蛋白与内参β-actin条带积分光密度值的比值反映目的蛋白的表达水平。
1.4.2 苏木精-伊红(HE)染色检测小鼠肺脏组织形态
将切好块的小鼠肺组织用PBS 清洗去除血渍,投人10%福尔马林固定液60min。通过梯度酒精(70%、80%、95%、100%)进行脱水,然后用二甲苯进行透明处理,浸蜡包埋后,将固定修好的石蜡块放在莱卡切片机载物台上,调整石蜡块与刀口的角。将切好的石蜡带放置于载破片上,烘干。通过梯度二甲苯、酒精进行脱蜡,将切片放人苏木精中染色10min,用自来水流水冲洗15min;再进行梯度酒精脱水,用0.5%伊红染色3min,用95%乙醇洗去多余的红色。最后放入无水乙醇、二甲苯I,II,III 各10min,利用中性树胶封存,显微镜下观察肺脏组织形态。病理学评分标准:1)肺泡充血和间质水肿:无异常为0分,轻度异常为1分,中度异常为2分,重度异常为3分;2)肺内出血:无红细胞为0分,极少数为1分,较多数为2分,充满肺泡腔为3分;3)肺泡腔或血管壁中性粒细胞浸润或聚集:无白细胞为0分,极少数为1分,较多数为2分,充满肺泡腔为3分;4)肺泡壁增厚和透明膜形成:无透明膜形成为0分,<20%肺泡出现透明膜为1分,20%~50%肺泡出现透明膜为2分,>50%肺泡出现透明膜为3分[19-20]。
1.4.3 采用双抗体夹心酶联免疫吸附试验(ELISA)检测血清肿瘤坏死因子(TNF)-α、白细胞介素(IL)−1β和IL−6水平
取−80℃保存的血清,按小鼠TNF−α,IL−1β和IL-6 ELISA试剂盒(美国R&D公司)操作步骤加样,用KHB ST-360酶标仪检测血清TNF−α,IL−1β和ⅡL-6炎症因子浓度。
1.4.4 免疫荧光染色检测GM130表达情况
将10%甲醛固定、石蜡包埋的肺组织切片用0.3% Triton X-100在PBS中渗透,用10%正常山羊血清阻断。用目标特异性一抗GM130在4℃下免疫染色过夜。第2天,清洗样品后,与相应的Alexa Fluor®488偶联的二抗在室温下孵育1h,并使用含有DAPI(美国Thermo Fisher Scientific公司)的延长黄金抗褪色安装液进行安装。所有样品用徕卡显微镜检查,用Image J软件分析。对于高尔基体形态学评估,碎片化高尔基体被定义为核周区域的分散点(不连接)或基于GM130染色的多个与高尔基体分离的迷你高尔基体(孤立点)。
1.5 统计学处理
数据使用GraphPad Prism 8.0软件进行统计分析。计量资料表示为均数±标准差,两组比较采用t检验,多组比较采用单因素方差分析,进一步两两比较采用Tukey's多重检验,P<0.05为差异有统计学意义。
2 结果
2.1 电针刺可显著减轻脂多糖诱导的肺高尔基体应激
LPS 组肺组织的CREB3 蛋白表达水平高于WT组(P<0.05),EA+LPS 组肺组织CREB3蛋白表达水平低于 LPS组(P<0.05)。与WT组相比,LPS组高尔基体应激相关蛋白Golgin97、GRASP65表达下调,而 GOLPH3 表达上调(P<0.05)。与 LPS 组相比,EA+LPS 组Golgin97蛋白、GRASP65蛋白表达上调,GOLPH3蛋白表达下调(P<0.05),而SEA+LPS 组上述各指标与LPS组差异无统计学意义(P>0.05),见图1。
2.2 电针刺通过CREB3缓解脂多糖诱导的高尔基体应激
与LPS+EA 组比较,CREB3−KO+LPS+EA组肺组织CREB3蛋白表达降低(P<0.05,图2A、2B),证明CREB3敲除小鼠制备成功。与LPS+EA组相比,CREB3−KO+LPS+EA 组Golgin97 蛋白、GRASP65蛋白表达上调,而GOLPH3蛋白表达下调 (P<0.05,图2C~2E)。荧光染色结果显示,LPS+EA 组的高尔基体结构在细胞质内碎裂成大量高强度点状结构向细胞质内扩散;而CREB3-KO+LPS+EA 组高尔基体变为更规整的相似带状结构(图2F)。
2.3 电针刺通过CREB3 缓解脂多糖诱导的炎症反应和肺损伤
脂多糖干预12h 内,LPS+EA 组与CREB3−KO+LPS+EA 组小鼠的体质量和体温无明显差异(图3A、3B)。与LPS+EA 组比较,CREB3-KO+LPS+EA组血清TNF−α,IL−1β、IL-6浓度、肺干湿比(W/D)值和肺损伤评分降低(P<0.05)(图3C~3G)。与LPS+EA 组比较,CREB3−KO+LPS+EA 组可显著减轻LPS刺激引起的肺泡壁增厚、出血、肺泡破坏和炎症细胞浸润(图3H),表明电针刺通过CREB3缓解LPS诱导的肺损伤,改善全身炎症反应。
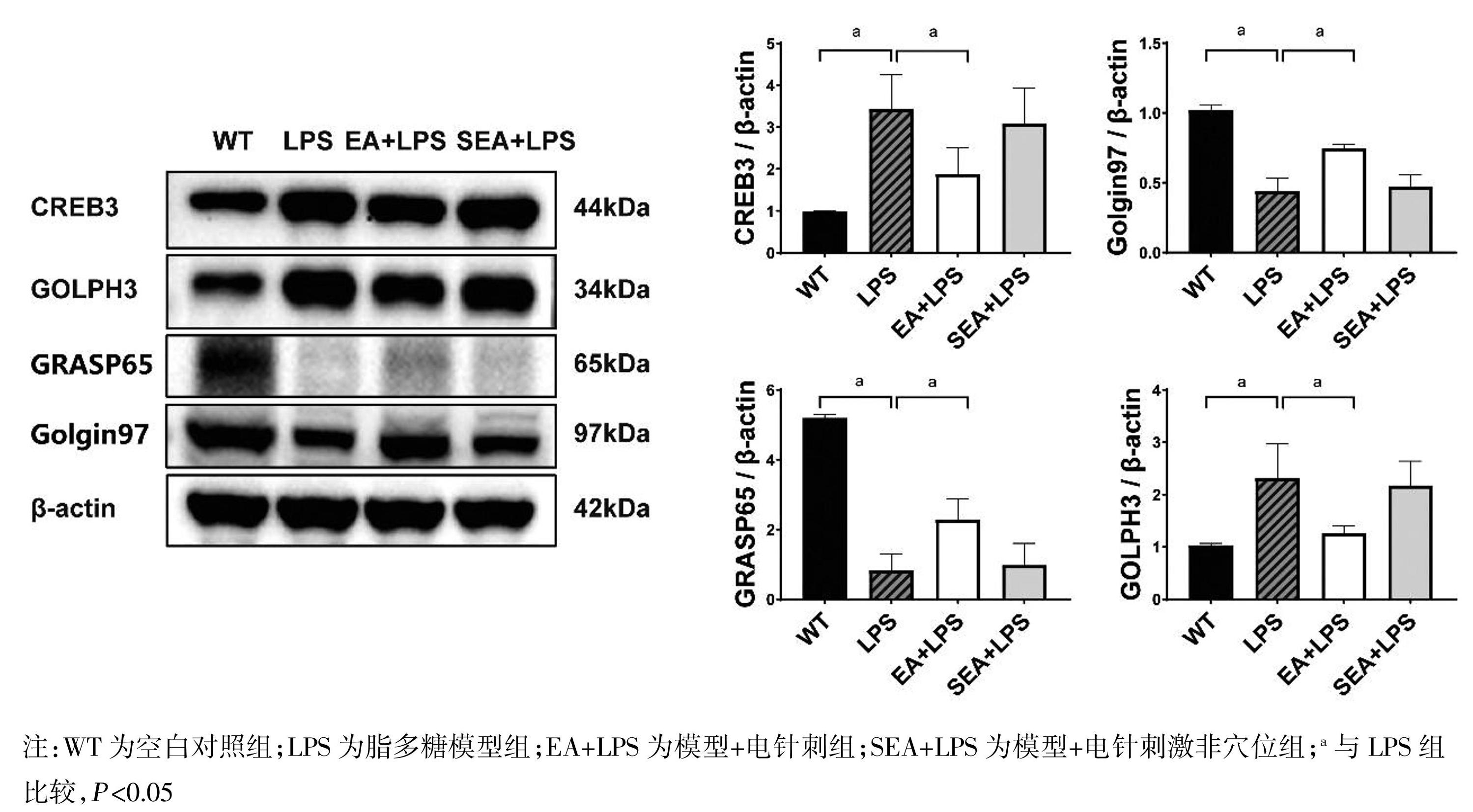
图1电针刺可显著减轻脂多糖诱导的肺高尔基体应激
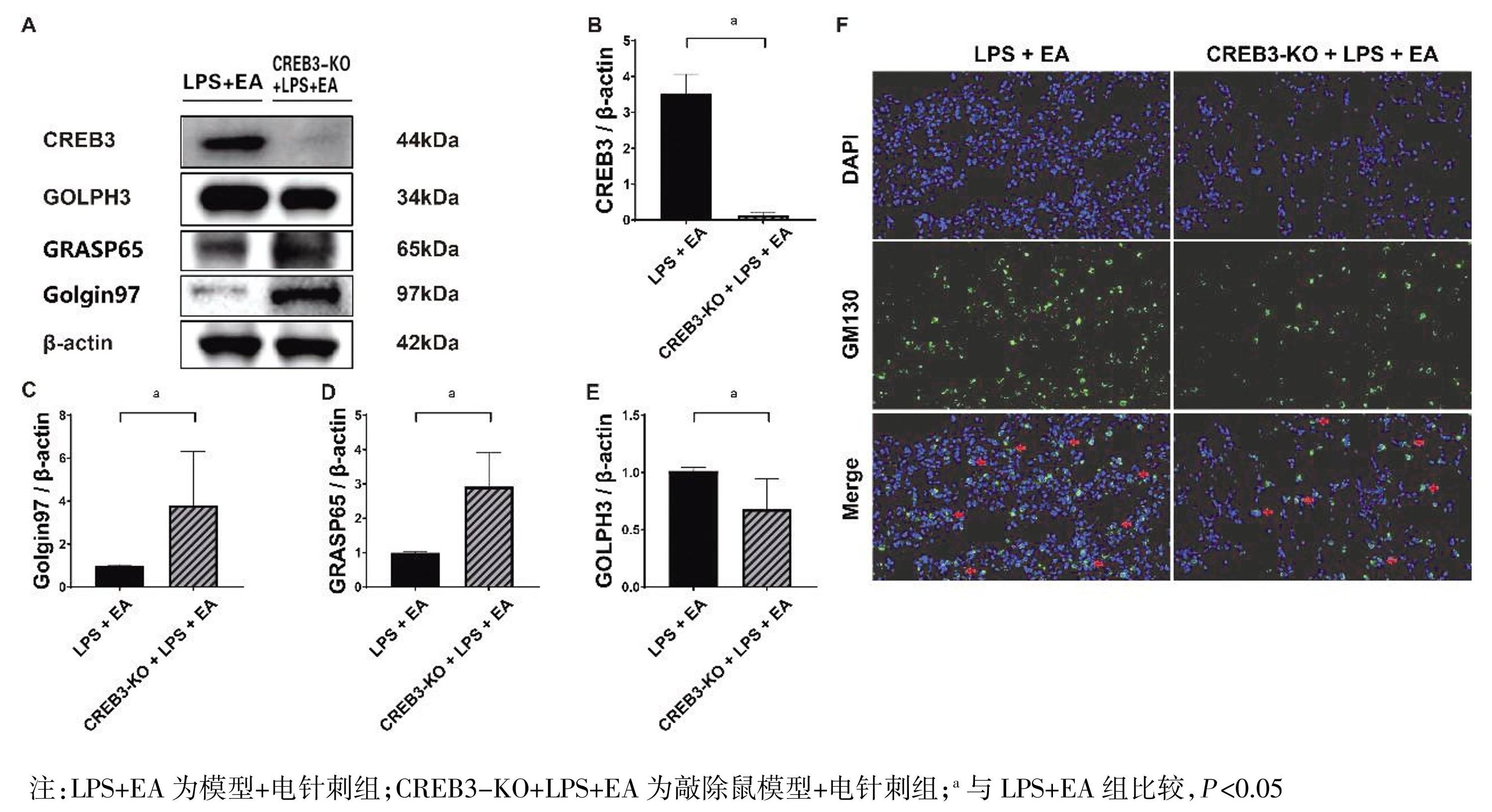
图2电针刺通过 CREB3 缓解脂多糖诱导的高尔基体应激
3 讨论
脓毒症仍然是危重患者死亡的主要原因[5]。有研究表明,电针刺可能通过显著的抗炎作用改善脓毒症进程[13,21]。本研究表明,在双侧足三里穴和肺俞穴处行电针刺治疗可显著减轻高尔基体应激、促进促炎细胞因子的产生和减轻内毒素急性肺损伤。EA 预处理显著改善了肺组织中LPS诱导的高尔基体碎裂和塌陷,EA的保护作用可能与抑制CREB3等关键蛋白有关,CREB3/ARF4是调节高尔基应激反应的主要机制之一。CREB3敲除小鼠可逆转电针刺对高尔基体应激、炎症反应及脓毒症肺损伤的治疗效果,但对小鼠体质量与体温似乎无影响。本研究的数据表明电针刺的肺保护作用部分通过高尔基体应激的关键通路CREB3/ARF4进行。
图3电针刺通过 CREB3 缓解脂多糖诱导的炎症反应和肺损伤
高尔基体应激反应是高尔基体作为细胞物质代谢核心的细胞器在面对细胞、亚细胞水平的有害刺激或疾病状况时所做出的适应性反应,表现为高尔基体碎裂等形态学改变,高尔基应激相关基因表达和蛋白水平的变化,高尔基体膜表面成分修饰等结构改变以及高尔基体膜离子泵活性等功能改变[22-23]。有研究表明,调控高尔基体的功能状态并抑制过度的高尔基体应激反应对辅助治疗肺部疾病具有十分重要的意义[24]。本研究发现,电针刺治疗可以帮助调整高尔基体的含量和容量,并满足细胞对细胞稳态的需求。电针刺治疗可显著抑制CREB3表达,恢复了脓毒症小鼠肺部高尔基体的形态,以达到对内毒素血症受损肺脏的保护作用。
CREB3是一种属于bZIP家族并定位于内质网膜的转录因子,可以促进高尔基体应激诱导的细胞凋亡[8]。在未发生高尔基应激时,CREB3 位于在内质网膜上;当发生高尔基应激时,CREB3被运输到高尔基体上并且被蛋白酶S1P、S2P 裂解,裂解后的CREB3从高尔基体膜释放并移位到细胞核激活靶基因的转录[25-26]。既往研究表明,高尔基体应激的重要转录因子CREB3表达及转录活性增强会促进乳腺癌的肺转移[12]。本研究结果表明,脓毒症时肺组织的CREB3被激活,提示CREB3通过介导高尔基体应激引发炎症扩大反应,导致内毒素急性肺损伤,而电针刺可逆转其表达。
本研究仍存在一些不足,内毒素血症和其他小鼠模型只能部分表现出与人类败血症不同阶段的分子相似性,本文采用的LPS造模法是一种定义明确的配体-受体途径,其优点在于可以精确分析且可重复性高;未来进一步采用盲肠结扎和穿刺(CLP)造模法研究电针刺对内毒素急性肺损伤的机制,有利于更全面且动态评价其影响。
综上所述,CREB3参与电针刺减轻小鼠内毒素急性肺损伤的作用,其机制可能与缓解高尔基体应激,从而抑制炎症反应相关。


